1
INTRODUÇÃO
O
solo é constituído por três fases: uma sólida, uma líquida e uma gasosa. A fase
sólida é composta de uma fração mineral e uma fração orgânica. Abordando a
composição da fração sólida mineral do solo, destaca-se que a importância do
conhecimento mais detalhado da fase sólida deve-se ao seu íntimo contato com a
fase líquida, a solução do solo. É da
solução do solo que as plantas retiram os nutrientes necessários ao seu
crescimento e desenvolvimento, mas é a fase sólida que controla, em grande
parte, a composição da solução do solo.
Os
minerais que estão presentes nos solos podem ser herdados, ou originam-se a
partir dos constituintes minerais das rochas pela ação dos fatores de formação
do solo ao longo do tempo (intemperismo). As rochas fragmentam-se,
dissolvendo-se e liberam elementos (cátions e ânions) que podem se organizar em
novas estruturas, originando novos minerais.
A composição mineralógica do solo depende do material de origem e do
grau de intemperização a que esteve submetido. Assim, solos de regiões
tropicais têm composição mineralógica bastante diferente da dos solos de
regiões temperadas, pois se desenvolvem sob condições quentes e úmidas,
favorecendo a presença de minerais em estádios mais avançados de intemperismo.
2
OS MINERAIS DO SOLO
Os
elementos encontrados em maiores quantidades em solos são o O, Si, Al, Fe, Ca,
K, Na, e Mg. O oxigênio é o elemento que prevalece, compreendendo cerca de 47%
do peso da crosta terrestre e 90% do seu volume (Tabela 1). Esses elementos compõem os minerais da fração
inorgânica do solo e, normalmente, representam mais de 90% da fase sólida, e
suas propriedades, como tamanho, área superficial e cargas elétricas, afetam
importantes processos e reações em solos.
Um
mineral é um sólido homogêneo, com uma composição química definida e um
arranjamento atômico ordenado. Os minerais são, primeiramente, divididos em
classes, dependendo do ânion ou do grupo aniônico dominante. As classes são: a)
elementos nativos, b) sulfitos, c) sulfosais, d) óxidos e hidróxidos, e)
haletos, f) carbonatos, g) nitratos, h) boratos, i) fosfatos, j) sulfatos, l)
tungstatos, m) silicatos. Essas classes são, então, subdivididas com base na
estrutura química e nas semelhanças na estrutura (Schulze, 1989).
Os
elementos nativos, sulfosais, nitratos, boratos e tungstatos, pertencem às
classes de minerais de menor importância em solos.
Os
minerais dos solos também podem ser divididos em minerais primários e minerais
secundários, com tamanho variando desde <0,002 mm até matacão e rochas (Figura
1).
Fonte:http://disciplinas.stoa.usp.br/pluginfile.php/130974/mod_resource/content/1/TextoSOloV5.pdf
Um
mineral primário é aquele que não foi
alterado quimicamente desde a sua deposição e cristalização da lava derretida.
Os minerais primários são formados em temperaturas elevadas e, em geral, são
derivados de rochas ígneas ou metamórficas, mas podem também ser herdados de
rochas sedimentares. Exemplos de minerais primários comuns em solos incluem o
quartzo e feldspatos. Outros minerais primários que podem ser encontrados em
solos, em menores quantidades, são piroxenos, micas, anfibólios e olivinas. Os
minerais primários ocorrem, principalmente, nas frações areia e silte, mas
podem, também, ser encontrados em frações da argila levemente intemperizadas. A
ocorrência dos minerais primários pode fornecer informações importantes, como
grau de evolução do solo e sua reserva mineral.
Um
mineral secundário é aquele
resultante da intemperização de um mineral primário, quer seja pela alteração
da estrutura, quer pela reprecipitação de produtos da intemperização de um
mineral primário. São formados por reações em baixas temperaturas, podendo
originar-se de rochas sedimentares ou de processos de intemperização dos solos.
Os minerais secundários comuns em solos são os aluminossilicatos, como a
caulinita e a montmorilonita; os óxidos, como a gibbsita; os materiais amorfos,
como o alofano, o enxofre e os carbonatos. As classes de minerais primários e secundários
não são mutuamente exclusivas, ocorrendo, em alguns minerais, em ambas as
classes.
2.1 PRINCIPAIS CLASSES DE
MINERAIS
As
principais classes de minerais que ocorrem em solos são apresentadas a seguir:
2.1.1 Minerais não
silicatados
a) Haletos,
Sulfatos e Carbonatos - é um grupo de minerais com estruturas
relativamente simples. As ligações entre os cátions e ânions que compõem as
suas estruturas são predominantemente iônicas. Os principais representantes
desse grupo são a halita (NaCl), o gesso (CaSO4.2H2O), a
calcita (CaCO3) e a dolomita [(CaMg)CO3]. Esses minerais
são muito solúveis e facilmente intemperizáveis. São encontrados em regiões
semiáridas, que têm baixa disponibilidade de água para intemperizá-los, e em
solos jovens de regiões mais úmidas onde os processos de intemperização tenham
sido mínimos.
b) Sulfitos – a
pirita (FeS2) é o principal mineral dessa classe, ocorre em solos
associada ao carvão ou em sedimentos marinhos nos depósitos orgânicos, causando
problemas de acidificação do solo com a sua oxidação, pela formação de ácido
sulfúrico (H4SO4).
c) Óxidos,
hidróxidos e oxihidróxidos - os minerais primários decompõem-se
durante os processos de intemperismo, liberando cátions e ânions que se
recombinam para formar outros minerais mais estáveis. Muitos elementos,
particularmente Al, Fe e Mn, formam óxidos, hidróxidos ou oxihidróxidos que são
estáveis em solos intemperizados, como em muitos solos brasileiros. Os óxidos
de alumínio e de ferro afetam importantes propriedades químicas dos solos.
Os
óxidos
de ferro ocorrem em maiores quantidades na fração argila dos solos. O
tipo de óxido que ocorre no solo reflete as condições ambientais que
determinaram a sua formação. Os óxidos de ferro são originários da decomposição
de minerais primários ferro-magnesianos, como olivinas, piroxênios e anfibólios
e são encontrados, principalmente, em rochas magmáticas básicas como o basalto.
O ferro liberado pelos minerais primários pode ser complexado pela matéria
orgânica, pode ser incorporado na estrutura dos minerais que estão se formando
por substituições isomórficas, pode ser precipitado sob a forma de
oxihidróxidos ou ainda ser absorvido pelas plantas.
Os
óxidos de ferro mais importantes são:
Goethita (FeOOH) – a
estrutura básica é constituída por cadeias duplas de octaedros de Fe-O-OH. É a
forma mineral mais estável dos óxidos de ferro em solos, ocorrendo em quase
todas as regiões e climas. A sua formação é favorecida, em regiões de baixas
temperaturas, quando no processo de intemperização há um baixo fluxo de íons de
ferro divalente (Fe2+) para o ambiente, condições de elevados teores
de umidade, de matéria orgânica, de pH ácido e de teores de alumínio trocável
elevado. Confere a coloração amarelada e marrom aos solos e pode ocorrer
associada à hematita. No estado do Rio Grande do Sul, ocorre predominantemente
na região dos Campos de Cima da Serra.
Hematita (Fe2O3) – a
estrutura básica é constituída também por octaedros de Fe, rodeado por seis
átomos de O e/ou OH. Formam-se em condições opostas às da goethita, em climas
quentes e úmidos, predominantemente de rochas com alta concentração de minerais
ferro-magnesianos. Apresenta alto poder de pigmentação, conferindo a cor
vermelha aos solos. A goethita e hematita são estáveis em solos oxidados e
instáveis em condições de redução.
Lepidocrocita (FeOOH) – é
menos frequente em solos que a goethita e a hematita. Ocorre em ambientes
hidromórficos (com excesso de água e deficiência de oxigênio), ou seja, em
solos de má drenagem.
Ferrihidrita (Fe10O15.9H2O) – constitui-se
de uma forma mal cristalizada de ferro, de coloração marrom, e ocorre em
situações de má drenagem (como na lavoura do arroz).
Magnetita –
tem propriedades magnéticas, podendo ser detectada nos solos com um ímã.
Maghemita – é
comum em solos altamente intemperizados dos climas tropicais.
Os
óxidos
de alumínio que podem ser encontrados em solos são a bayerita, a
boehmita, a diáspora e a gibbisita. O óxido de alumínio mais importante é a gibbisita Al(OH)3, cuja
estrutura, cristalina e octaédrica, é constituída de dois planos de OH-
com íons Al3+ entre eles (Figura 3). É o óxido de alumínio mais
importante em solos, encontrado com frequência nos solos intemperizados das
áreas tropicais. No Brasil, ocorre comumente em Latossolos do estado de Goiás e
do Distrito Federal.
Os
óxidos
de manganês estão, na sua maioria, em formas cristalinas, podem
adsorver metais pesados, e são os oxidantes naturais de metais, como o As3+
e o Cr3+.
Óxidos
de titânio – são muito resistentes ao intemperismo. Os
mais comuns são o anatásio e o rutilo, que praticamente, não têm importância
agrícola. São úteis para a identificação e classificação de solos e materiais
de origem.
a) Fosfatos –
esses minerais ocorrem em pequena porcentagem da fase sólida do solo. São
formados sob as mais diferentes condições ambientais. Podem se apresentar em
inúmeras estruturas, em formas cristalinas e não-cristalinas. A apatita é o
mineral fosfatado mais frequentemente identificado em solos, e sua
intemperização dá origem a várias espécies de minerais fosfatados secundários.
Em geral, os fosfatos cristalinos são utilizados para a fabricação de
fertilizantes fosfatados solúveis, pela sua acidulação com ácidos fortes (em
geral o H2SO4). Os não-cristalinos são utilizados para
aplicação direta aos solos. No Brasil, existem extensas jazidas de fosfatos
cristalinos, como as de Araxá e de Pato de Minas, por exemplo. As jazidas de
fosfatos naturais mais importantes para a aplicação direta ao solo são
encontradas na África e em Israel.
2.1.2 MINERAIS SILICATADOS
A
classe dos minerais silicatados constitui um importante grupo dos minerais em
solos, uma vez que cerca de 40% dos minerais comuns são silicatados. Constituem
mais de 90% da crosta terrestre e ocorrem tanto em minerais primários, herdados
de rochas ígneas ou metamórficas, como em minerais secundários, formados pela
intemperização dos produtos dos minerais primários.
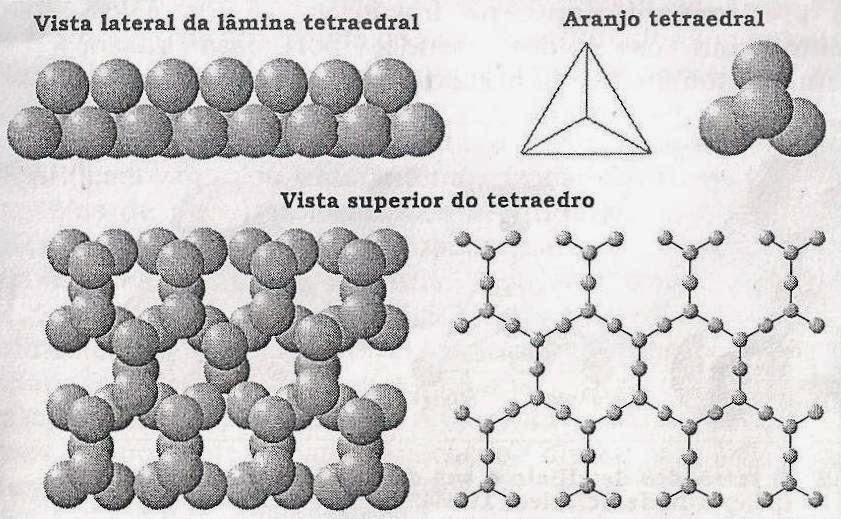
A
unidade fundamental de formação de um mineral silicatado é o tetraedro de
silício (SiO4). Ele consiste em quatro átomos de O2- coordenados
por um átomo de Si4+, no centro (Figura 4). Os tetraedros
individuais ligam-se uns aos outros pelo compartilhamento dos íons O2-,
formando estruturas mais complexas. O tetraedro pode estar presente nos
minerais como um único tetraedro (nesossilicatos), como tetraedros duplos
(sorossilicatos), unindo-se na forma de anéis (ciclossilicatos), na forma de
cadeias simples ou duplas (inossilicatos), organizando-se em camadas
constituídas do empilhamento de lâminas tetraedrais unidas a lâminas
octraedrais (filossilicatos), ou organizados em estruturas tridimensionais
(tectossilicatos) (Tabela 2). Os filossilicatos ocorrem predominantemente na
fração argila dos solos, juntamente com os óxidos, sendo, por essa razão,
comumente denominados argilominerais.

Os
principais minerais silicatados que ocorrem os solos são:
a) Nesossilicatos –
esses minerais são constituídos basicamente de tetraedros isolados de silício,
ligados por Mg ou Fe. O principal representante da classe é a olivina, comum em rochas magmáticas e
metamórficas. Apresenta-se com coloração escura, sendo de fácil decomposição.
b) Inossilicatos
–
apresentam estrutura em forma de cadeias simples ou duplas de tetraedros
isolados se silício, ligadas a cátions. São minerais escuros encontrados em
rochas básicas, como o basalto. São de decomposição rápida, liberando cátions,
como Mg, Ca, Fe, além de Al, Si e O, que podem formar novos minerais.
Destacam-se nesta classe os piroxênios e
os anfibólios.
c) Sorossilicatos
–
a estrutura desses minerais é constituída de duplos tetraedros de silício
unidos por um átomo de oxigênio basal, compartilhado. Exemplos da classe são as
melilitas e o epidoto.
d) Ciclossilicatos –
são consituídos de tetraedros de silício em estruturas de anéis fechados.
e) Tectossilicatos - a
estrutura dos minerais dessa classe apresenta empilhamento de tetraedros de
silício em arranjo tridimensional. Os representantes mais comuns da classe são
o quartzo e os feldaspatos.
O
quartzo é o mineral mais comum na
fração areia dos solos; é incolor e resistente ao intemperismo. Sua importância
está mais associada à parte física do solo, influenciando a sua textura (quanto
mais quartzo, mais arenoso é o solo). Está presente em rochas graníticas,
metamórficas e sedimentares.
A
estrutura dos feldspatos consiste no
empilhamento de tetraedros de silício em arranjo tridimensional, como no
quartzo; em alguns tetraedros ocorre, entretanto, substituição do Si4+ por
Al3+, e a carga negativa resultante é neutralizada por cátions K+,
Na+, Ca2+, entre outros, originando os diferentes
feldspatos. São minerais de cores claras, comuns nas frações areia e silte dos
solos, podendo também aparecer na fração argila. Ocorrem em rochas ígneas e
metamórficas. Os feldspatos podem ser potássicos (ortoclásio, K2OAl2O36SiO2)
ou calco-sódicos (plagiocásios: Na2OAl2O36SiO2
– albita, e CaAl2O32SiO2 – anortita). São
importantes porque liberam, na sua decomposição, nutrientes para as plantas,
como o K e o Ca e outros íons (Al, Si, O) que podem dar origem a minerais
secundários.
Quanto
aos filossilicatos, devido à especial importância no solo, sua abordagem será
realizada em separado.
2.1.3.
MINERAIS FILOSSILICATOS
Os filossilicatos são os minerais que
predominam na fração argila dos solos e apresentam estruturas formadas pela
sobreposição de lâminas de tetraedros de silício, formando camadas que podem se
empilhar sucessivamente, como nas folhas de um livro (daí a origem do nome de filossilicatos). O empilhamento dessas
camadas, que é variável, e a extensão do empilhamento determinam o tamanho do
cristal e o tipo de mineral que é formado. Os principais minerais desse grupo
são as micas, a caulinita, as esmectitas, a vermiculita, a ilita e a clorita.
Para melhor compreensão da estrutura dos filossilicatos, deve-se considerar que os átomos tenham a forma esférica, isto é, que sejam esferas com diferentes tamanhos. A melhor forma de “acomodar” as esferas num plano é dispondo-as num arranjo hexagonal (Figura 5). Colocando um outro plano de esferas sobre o primeiro. Este naturalmente se “encaixará” nos espaços existentes entre as esferas do primeiro plano hexagonal. Os espaços existentes entre as esferas maiores (átomos de O2-) dos dois planos superpostos são ocupados por esferas de raio bem menor (átomos de Si4+ e Al3+), compartilhando elétrons de modo a satisfazer as necessidades das duas figurações eletrônicas. O átomo de Si4+ pode coordenar quatro átomos de oxigênio ao seu redor, num arranjo tetraedral (Figura 5). O átomo de Al3+ pode coordenar seis oxigênios (três de cada plano) ao seu redor, num arranjo octaedral (Figura 5.1).
Para melhor compreensão da estrutura dos filossilicatos, deve-se considerar que os átomos tenham a forma esférica, isto é, que sejam esferas com diferentes tamanhos. A melhor forma de “acomodar” as esferas num plano é dispondo-as num arranjo hexagonal (Figura 5). Colocando um outro plano de esferas sobre o primeiro. Este naturalmente se “encaixará” nos espaços existentes entre as esferas do primeiro plano hexagonal. Os espaços existentes entre as esferas maiores (átomos de O2-) dos dois planos superpostos são ocupados por esferas de raio bem menor (átomos de Si4+ e Al3+), compartilhando elétrons de modo a satisfazer as necessidades das duas figurações eletrônicas. O átomo de Si4+ pode coordenar quatro átomos de oxigênio ao seu redor, num arranjo tetraedral (Figura 5). O átomo de Al3+ pode coordenar seis oxigênios (três de cada plano) ao seu redor, num arranjo octaedral (Figura 5.1).
Planos
de tetraedros de Si4+ (lâminas) e planos de octaedros de Al3+
(lâminas), superpostos, formam camadas que compõem a estrutura básica de
diversos minerais filossilicatos em solos. Na figura 5.2, são apresentadas
essas estruturas e sua representação através de diferentes tipos de modelos.
Na
formação dos filossilicatos, quando uma lâmina de tretraedros de Si se une a
uma lâmina de tetraedros de alumínio, formando uma camada que se repete de
forma idêntica no empilhamento, origina-se um mineral denominado do tipo 1:1. Na formação dos filossilicatos
também pode ocorrer um empilhamento, de maneira que uma lâmina de octaedros de
alumínio fique entre duas lâminas de tetraedros de silício (como num
sanduíche), ficando, dessa forma, a camada constituída de duas lâminas de
silício para uma de alumínio, dando origem, assim, aos minerais do tipo 2:1.
Figura
5 - Lâmina tetraedral vista sob diferentes ângulos e diferentes formas de
representações.
Fonte:
Adaptado de (Schulze, 1989).
Figura
5.1 - Lâmina octaedral vista sob diferentes ângulos e diferentes formas de
representações.
Fonte:
Adaptado de (Schulze, 1989).
Figura
5.2 – Lâminas tetraedrais e octraedrais constituindo as camadas de
argilominerais do tipo 1:1 e tipo 2:1.
Figura
5.3 – Para a melhor compreensão de como funciona o arranjo dos átomos no plano
hexagonal, elaborou-se arranjos simples das unidades básicas de formação dos
minerais usando esferas de diferentes tamanhos (bola de sinuca, bolinha de gude
e esfera automotiva). Utilizou-se paquímetro digital para medir as esferas e
possivelmente explicar a influência do raio do átomo no processo de formação e
compartilhamento de elétrons nas possíveis camadas. Observa-se que não há o
“encaixe” perfeito das esferas menores entre as esferas (“átomos”) maiores.
Se
as ligações entre as camadas não são fortes, elas podem se expandir quando
hidratadas (como numa gaita de foles), e o mineral é dito expansível. Por outro lado, se as ligações entre as camadas forem
fortes, impedindo a sua separação, os minerais formados não serão expansíveis.
Os principais filossilicatos que ocorrem na fração argila do solo são os
seguintes:
a) Caulinita - constituída por lâminas
tetraedrais de Si4+ ligadas a lâminas octaedrais de Al3+,
através do compartilhamento dos oxigênios apicais dos tetraedros (Figura 6),
sendo, portanto, um mineral do tipo 1:1. A caulinita é um mineral secundário do
solo, sendo formado pela intemperização dos feldspatos e das micas. A caulinita
é o principal argilomineral presente na maioria dos solos ácidos tropicais e
subtropicais, juntamente com os óxidos de ferro e alumínio.
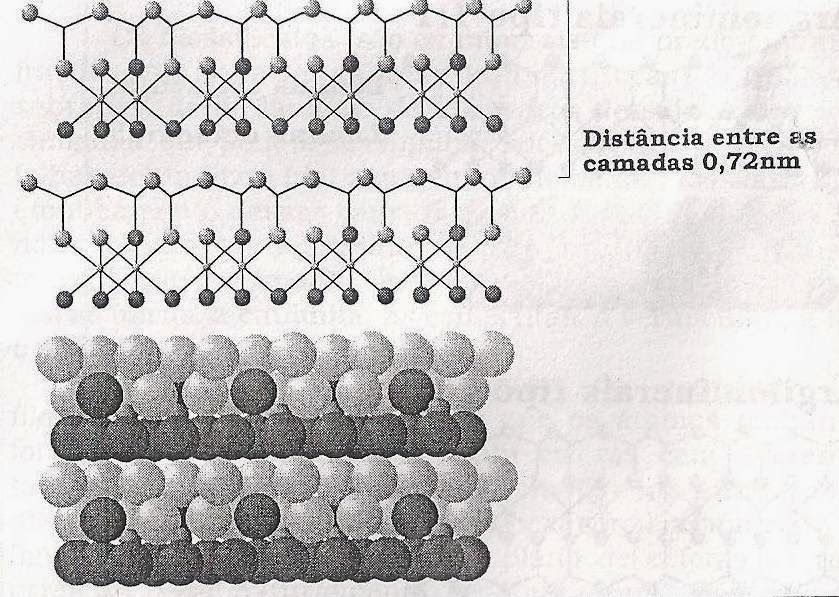
Devido
à ligação forte entre as camadas (ligações O-OH ou pontes de hidrogênio), o
mineral não é expansível, mantendo uma distância fixa entre as camadas de 0,75
nm.
Figura
6 -
Estrutura
cristalina da caulinita demonstrando a distância de 0,72 nm entre as camadas.
Fonte:
Adaptado de (Schulze, 1989).
A fórmula química típica da caulinita é Al4Si4O10(OH)8.Observa-se que o número de cargas positivas nesse mineral [4 x Al3+ + 4 x Si4+ = (4 x 3) + (4 x 4) = 28 ] é exatamente igual ao número de cargas negativas [10 x O-2 + 8 x OH-1 = (10 x -2) + (8 x -1) = - 28], resultando numa estrutura neutra (+ 28 - 28 = 0). Entretanto, podem ocorrer cargas negativas nas bordas desses minerais pela dissociação de prótons H+ do grupo OH-. Devido à neutralidade da estrutura desse mineral e ao fato de o aparecimento das cargas na sua periferia não serem muito significativa, os solos em que a caulinita é predominante, como, por exemplo, os Latossolos brasileiros, apresentam baixa capacidade de troca de cátions. Por outro lado, por serem minerais não expansivos, promovem boas características físicas ao solo (agregação, aeração, drenagem).
Figura
6.1 – Modelo estrutural da caulinita (argilomineral do tipo 1:1).
b) Haloisita -
sua estrutura é semelhante à da caulinita, isto é, do tipo 1:1, podendo
apresentar, porém, moléculas de água estruturais entre as camadas, o que
expande a distância entre elas para 1,0 nm. É menos frequente em solos,
ocorrendo principalmente em solos derivados de depósitos vulcânicos.
c) Micas -
as micas são argilominerais do tipo 2:1, isto é, constituídas de uma lâmina
octaedral de Al entre duas lâminas tetraedrais de Si (Figura 6.2). Os cátions
encontrados na lamina octaedral são o Al, o Mg e o Fe. Se o cátion que ocupar o
centro dos octaedros for trivalente, somente duas das três posições possíveis
nas lâminas octaedrais podem ser ocupadas, sendo a lâmina denominada de
dioctaedral. Se o cátion é divalente, as três posições são ocupadas, e a lâmina
é denominada trioctaedral.
Nos
tetraedros de silício pode haver substituição de Al³+ por Si4+,
originando, assim, cargas negativas nesse mineral, as quais são compensadas
parcialmente pelo cátion K+ nas entrecamadas, com ligação forte, o
que impede a sua expansão. As micas apresentam uma distância basal fixa de 1,0
nm entre as camadas.
As
micas são minerais primários do solo, e as mais comuns são a muscovita
(dioctaedral), de coloração branca e a biotita (trioctaedral), de coloração
escura. A muscovita (K2O3Al2O3.6SiO2.2H2O)
decompõe-se lentamente no solo e é encontrada em diversas rochas, como granito,
gnaisse e micaxisto. A biotita K(Fe, Mg)3 Si3AlO10
(OH)2 também pode ser encontrada no granito, no gnaisse e no
micaxisto, sendo de decomposição mais fácil. As micas são importantes fontes de
potássio no solo.
Figura
6.2.1 – Estrutura trioctaedral da Biotita e estrutura dioctaedral da muscovita.
d)
Ilita - apresenta uma estrutura
muito semelhante à da mica. Sendo denominada também de mica hidratada, por
apresentar moléculas de água na estrutura. A ilita é menos cristalina que a
mica e contém menos potássio. Não apresenta expansão entre as camadas e o
espaçamento entre ela é fixo, de 1,0 nm.
Figura
6.3 - Representação (com esferas) da estrutura da Ilita. As esferas amarelas na
entrecamada representam íons K+.
e)
Vermiculita - é um argilomineral do tipo 2:1 derivado da transformação das micas
pelo intemperismo. A vermiculita apresenta maior substituição isomórfica na
camada tetraedral (Al³+ substitui o Si4+), originando um
excesso de cargas negativas que vão se manifestar na superfície interna do
mineral, nas entrecamadas, A vermiculita é expansível, e o espaçamento entre as
camadas é de 1,4 nm, podendo variar de 1,0 nm, quando retém o íon K+
entre as camadas, ou até cerca de 1,5 nm, quando existem moléculas de água e
cátions hidratados nas entrecamadas (Figura 6.4). Devido à expansão, a
superfície interna das entrecamadas fica exposta, o que aumenta
significativamente a área superficial especifica (em torno de 750 g m-²)
e a CTC desse mineral, que é de aproximadamente 160-200 cmolc Kg-¹,
das quais mais de 95% localizam-se na superfície interna do argilomineral.
A
capacidade de expansão e de contração da vermiculita confere aos solos
características de plasticidade e de pegajosidade, o que dificulta o manejo
agrícola dos solos, onde ocorre em quantidades significativas.
Figura 6.4 - Estruturas da Montmorilonita
(2:1 dioctaedral) e da Vermiculita (2:1 trioctaedral) com presença de cátions
trocáveis nas entrecamadas.
f)
Clorita - não é tão abundante como
outros argilominerais em solos. É menos estável em condições de solos ácidos e
pode ser rapidamente alterada. Apresenta uma estrutura formada por quatro
lâminas de poliedros. Três lâminas são unidas quimicamente para formar uma
camada 2:1, estruturalmente semelhante à da mica. A quarta lâmina têm estrutura
de hidróxi entrecamadas, como gibbsita [(Al(OH)x] ou como brucita
[(Mg(OH)x]. Devido a essa estrutura, muitas vezes é referida como
uma argila 2:1:1.
A
clorita apresenta, geralmente, coloração esverdeada, sendo herdada de minerais
primários encontrados em rochas metamórficas ou rochas ígneas. Pelo
intemperismo, a clorita forma a vermiculita e as esmectitas.
Figura 6.5 – Estrutura cristalina da clorita.
g)
Esmectitas - os principais minerais
desse grupo são a montmorilonita, a beidelita e a nontronita; são minerais do
tipo 2:1. As substituições isomórficas do Al³+ por Fe²+ e
Mg²+, na lâmina octaedral, dão origem às cargas negativas, que vão
se manifestar na superfície do mineral, sendo, por isso, mais fracas. Assim, as
esmectitas podem expandir mais do que a vermiculita: a distância entre as
camadas varia de 1,0 a 2,0 nm. Apresentam alta CTC (de 80 a 120 cmolc
Kg-¹) e grande expansividade das camadas permite a entrada de
cátions hidratados, de moléculas de água e de moléculas orgânicas polares, como
as de herbicidas e fungicidas, por exemplo.
Devido
às características de expansão e contração, causam problemas de manejo nos
solos onde ocorrem: quando úmido, são muito plásticos e pegajosos e, quando
secos, ficam muito duros e com fendilhamentos. Em solos escuros da região
Campanha do estado do Rio grande do Sul, as esmectitas são argilominerais
predominantes. A montmorilonita é o mineral mais expressivo do grupo, e sua
fórmula típica é Mx(Si8)Al3,2Fe0,2Mg0,6O20(OH)4,
onde x, a carga líquida da camada, varia de 0,5 – 1,2.
h)
Minerais 2:1 HE - são minerais
semelhantes aos do tipo 2:1, porém com uma diferença importante, o que se deve
à deposição de polímeros de alumínio nas entrecamadas do mineral (Figura 2.9).
Podem se originar de outros argilominerais, como, por exemplo, da vermiculita e
das esmectitas. São identificados pela terminação HE (hidróxido entrecamadas).
Assim uma esmectita como hidroxi-Al entrecamadas é grafada como EHE; uma
vermiculita, como VHE.
A
lâmina octaédrica do polímero de alumínio que se deposita nas entrecamadas do
mineral, parcial ou totalmente, é fortemente retida, bloqueando o acesso à
superfície interna do mineral, o que reduz a sua CTC (10 a 40 cmolc
Kg-¹) e não permite a sua expansão, mantendo um espaçamento fixo de
1,4 nm. Nos solos ácidos do Brasil é comum encontrar-se esse tipo de mineral.
i)
Argilominerais interestratificados –
minerais estratificados ocorrem com frequência em solos. Apresentam, simultaneamente,
estrutura de dois ou mais minerais distintos, como, por exemplo, mica-ilita,
ilita-montmorilonita, mica-ilita-vermiculita. Isso ocorre devido a
transformações parciais do mineral original em um novo mineral. Os minerais
interestratificados apresentam, assim, propriedades diferentes nas porções
correspondentes do mineral, podendo, por exemplo, ser expansivo em determinada
porção, e não-expansivo em outra.
Os
principais argilominerais do tipo 2:1 têm características que são importantes
para os solos agrícolas, destacando-se: a) substituição isomórfica; b) alta CTC
independente do pH (cargas permanentes); c) alta área superficial especifica;
d) expansividade (exceções: minerais 2:1 HE e ilita).
Os
argilominerais do tipo 2:1 são mais comuns em regiões de climas temperados e
não são estáveis em ambientes quentes e úmidos, como nas regiões tropicais,
sendo de pouca ocorrência nessas regiões. Na região sul do Estado do Rio Grande
do Sul, na fração argila de algumas unidades de solos, frequentemente ocorre argilominerais
do tipo 2:1.
Figura 6.6 – Argilomineral interestratificado
com presença simultânea de dois minerais distintos do tipo 2:1 e tipo 2:1:1.
j)
Outros aluminossilicatos - outros
minerais aluminossilicatados de menor importância são a alofana e a imogolita,
os maiores componentes de solos vulcânicos, como os da América Central, do
Japão e do Hawai. A alofona é constituída por quantidades variáveis de O²-,
OH-, Al³+ e Si4+, apresentando-se em forma de
partículas esféricas. A imogolita é constituída por partículas que são
agregados de pequeníssimos tubos paralelos (cerca de 20 nm de diâmetro). Uma
característica importante é a grande capacidade que apresentam de reter o
fósforo, diminuindo acentuadamente a sua disponibilidade para as plantas.
2.4 ORIGEM DAS CARGAS
ELÉTRICAS NOS MINERAIS
a)
Substituição isomórfica – durante a
formação dos minerais, ocorrem substituições nas estruturas de um ou mais Íons
por outros. Um exemplo conhecido é o caso da Dolomita, um calcário magnesiano
onde Íons Mg²+ substituem Íons Ca²+. A substituição de um
Íon por outro num cristal, conservando a mesma estrutura, é denominada de
substituição isomórfica, devido a semelhança dos raios iônicos dos Íons que
substituem e dos que são substituídos.
As
substituições isomórficas ocorrem, com muita frequência, na formação dos
silicatos, e geralmente outros cátions, com raios iônicos semelhantes ao do
silício e ao do alumínio, podem substituí-los nas lâminas tetraedrais e
octaedrais. O mais comum é o Si4+ ser substituído por Al³+,
na lâmina tetraedral, e o Al³+ ser substituído por Mg²+ e
Fe²+, na lâmina octaedral. No tetraedro de Si, assim como no
octaedro de Al, as cargas dos íons de Si4+ (tetravalente) e do Al³+
(trivalente) são contrabalanceadas pelas cargas negativas dos oxigênios que a
eles se ligam. Assim, se na substituição isomórfica um íon de menor carga
substituir um de maior carga, haverá desbalanceamento de cargas no mineral,
havendo, nesse caso, um excesso de carga negativa, que se manifesta na
superfície do mineral.
As
cargas negativas que se originam nos silicatos pela substituição isomórfica,
durante a sua formação, são cargas
permanentes, não sendo afetadas por mudanças do pH do solo, pois se
originam na estrutura do mineral. A existência de cargas negativas nos argilominerais
do solo é, provavelmente, uma de suas propriedades mais importantes, pois,
graças a ela, o solo pode reter (adsorver) e trocar cátions com a solução do
solo, como Ca²+, Mg²+, K+, NH4+
entre outros, que são indispensáveis à nutrição das plantas. Essa propriedade é
denominada capacidade de troca de cátions do solo (CTC). Outros minerais do
solo, principalmente óxidos de alumínio e ferro tem a propriedade de apresentar
cargas positivas e negativas, conforme o pH do solo (cargas dependentes de pH).
b)
Cálculo da carga e da CTC de um
argilomineral – para exemplificar o cálculo da carga da camada e da CTC do
mineral, consideramos a fórmula química de uma vermiculita dioctaedral, onde
ocorrem substituições isomórficas tanto na lâmina tetraedral como na octaedral,
Para
a fórmula química (2.1), Mx representa a carga da camada.
Mx
(Si+4 5,7Al+³2,3) (Al+³0,5
Mg+²4,8 Fe+³0,7) O20 (OH)4 (2.1)
O
cálculo da carga pode ser efetuado da seguinte forma:
a)
A carga na lâmina tetraedral (2.2):
Si(5,7x4) + Al (2,3 x 3) = + 29.7
(2.2)
b)
carga da lamina octaedral (2.3):
Al
(0,5 x 3) + Mg (4,8 x 2) + Fe (0,7 x 3) + O (20 x - 2) + OH (4x-1) = -
30,8 (2.3)
Sendo,
portanto, a carga líquida da camada X = + 29,7 – 30,8 = - 1,10 equivalentes de
carga (1100 cmolc Kg-¹), Está é a carga que irá se
manifestar na superfície do mineral, sendo contrabalanceada por cátions da
solução do solo. Vê-se que a vermiculita tem uma alta carga na camada, o que
explica a alta CTC que apresenta. Pode-se, portanto, escrever, especificando a
carga líquida (x = 1,1) (2.4):
M1,1
(Si+4 5,7 Al+³ 2,3) (Al+³
0,5 Mg+² 4,8 Fe+³ 0,7) O20
(OH)4 (2.4)
Conhecendo-se
a carga líquida desse mineral, podemos calcular a sua CTC. A massa molecular da
vermiculita, para a fórmula acima é:
|
Si4+ 5,7
|
=
|
5,7 x 28,1
|
=
|
160,17
|
|
|
Al³+ 2,3
|
=
|
2,3 x 27,0
|
=
|
62,10
|
|
|
Al³+ 0,5
|
=
|
0,5 x 27,0
|
=
|
13,50
|
|
|
Mg²+ 4,8
|
=
|
4,8 x 24,3
|
=
|
116,64
|
|
|
Fe³+ 0,7
|
=
|
0,7 x 55,8
|
=
|
39,06
|
|
|
O²- 20
|
=
|
20,0 x 16,0
|
=
|
320,00
|
|
|
(OH)4 -
|
=
|
4,0 x 17,0
|
=
|
68,00
|
|
|
Total
|
=
|
779,50
|
gramas
|
Assim,
se em 779,50 gramas tem-se 1,1 equivalentes de carga em 1.000,0 gramas,
ter-se-á X. Efetuando-se tem-se que X = 1,41 equivalentes por quilograma de
vermiculita, (1.410 miliequivalentes de carga por quilograma), que se expressa,
de acordo com o sistema de unidades internacionais (SI), como 141,1 cmolc
Kg-¹. Assim a CTC desse mineral será de 141 cmolc Kg-¹.






















7 comentários:
Olá, poderia disponibilizar a referência dessa postagem?
Também gostaria das referências, por favor.
Boa tarde, sou completamente leigo nesse assunto, no caso "formação dos minerais que compõem o solo". Entretanto tenho uma dúvida, na verdade duas: primeiro a queda de corpos celestes como os meteoritos pode ser considerada como um agente de erosão? Considerando o tempo de formação da crosta terrestre é possível identificar algum tipo de mineral cuja formação foi decorrente desse tipo de fenômeno? (no caso queda de meteoros ou outros corpos celestes)
Agradeço desde já a atenção.
Para queria as referencias eu diria que foram os livros:Decifrando a terra; guerra e 19 lições de Pedologia, Igo Lbisch, pelos os conteudos disposto nesse trabalho, quanto ao que bora disse vc precisa entender que o processo de erosão é composta de três etapas; DESAGREGAÇÃO, TRANSPORTE E SEDIMENTAÇÃO, no caso de meteoros no geral elas dispersam em pequenas particulas quando atingem o solo, nesse caso pode se misturar o solo e até alterar a composição de minerais e rochas com adição, além disse a erosão é processo natural, exceto quando ocorre sob a infuência antrópica do homem . Agora se for o caso de um asteróide que formou uma cratera poderemos ter termos vários processos fisícos , químicos e mecânicos oriundos do impacto do asteróide com o solo, adição de novos elementos desagregação de particulas, temperatura gerada pelo asteroíde e etc.
Olá,
Boa noite.
Poderia me enviar as referencias para produção desse material.
Obrigado.
como ja dito acima, os livros usados foram : 1) Decifrando a terra; 2) guerra e 19 lições de Pedologia, Igo Lbisch
Postar um comentário